细菌耐药性已成为全球性健康危机,开发新型抗菌材料迫在眉睫。天然抗菌肽凭借独特的膜破坏机制可有效规避细菌耐药性,但存在合成成本高、酶稳定性差、生物利用度低等应用瓶颈。自组装纳米抗菌肽(nano-AMPs)可通过纳米结构提升代谢稳定性,并依靠高表面电位增强与细菌膜的静电结合,有效弥补传统抗菌肽的不足。然而,自组装纳米抗菌肽的高表面电位在提升抗菌活性的同时,也会导致其对哺乳动物细胞的亲和力增加,引发显著的细胞毒性和溶血反应。现有策略(如电荷屏蔽)虽能提升生物相容性,却往往大幅牺牲抗菌效力。因此,亟需发展全新设计思路同步实现高抗菌活性与高生物安全性,解决“活性-生物相容性固有悖论”。
针对这一关键难题,李文教授团队提出了一种“进攻-防御”一体化创新策略:一方面抑制纳米抗菌肽与哺乳动物细胞的非特异性结合(防御),另一方面强化其对细菌细胞膜的高效插入与破坏能力(进攻),实现抗菌活性与细胞毒性的有效解耦。该方案依托细菌与哺乳动物细胞膜天然的电荷差异,通过序列精准优化,引入丝氨酸(Ser)残基替代天冬酰胺(Asn)/谷氨酰胺(Gln)残基,同时合理调配疏水氨基酸组成,调控纳米组装体形成中等表面电位(约+20 mV)与松散分子堆积结构。适中电位可实现对带负电细菌膜的偏好结合,大幅降低与哺乳动物细胞的相互作用;而松散的堆积结构能够充分暴露疏水残基,显著提升抗菌肽对细菌膜的插入与破坏能力。
经优化得到的寡肽Ac-RFSFSVSFR-NH2(P7),对金黄色葡萄球菌和大肠杆菌的最低抑菌浓度(MIC)分别低至6 μM和5 μM,治疗指数(TI = HC10/MIC)>30,选择性指数(SI = IC20/MIC)>50,兼具优异抗菌活性、极低溶血副作用与良好细胞安全性。在小鼠皮肤伤口感染模型中,P7显著减少细菌负荷、促进伤口愈合、减轻炎症反应(降低IL-6和TNF-α),并展现出良好的组织相容性与生物安全性。该工作通过精准调控表面电位与疏水残基暴露程度,成功解耦了抗菌活性与生物相容性之间的矛盾,为纳米抗菌肽的合理设计提供了新的思路。
该研究成果以“Self-Assembling Nano-Antimicrobial Oligopeptides With Dual Offense–Defense Functions for Synchronously Achieving High Activity and Biosafety”为题发表在Angewandte Chemie International Edition上(Angewandte Chemie International Edition, 2026; 0:e5517893)。袋鼠影视
博士研究生赵鹤为第一作者,袋鼠影视
李文教授、中国石油大学(华东)徐海教授、韩国高丽大学Yongju Kim教授为共同通讯作者。
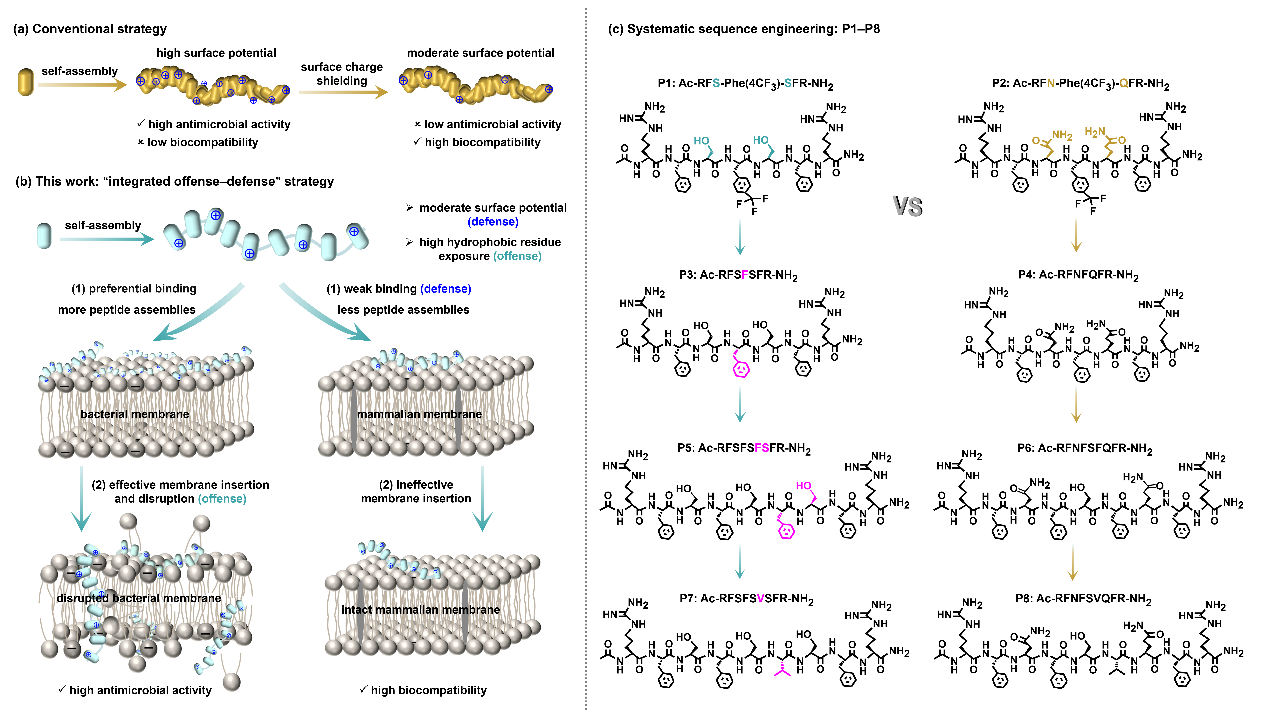
“攻防一体化”策略实现高抗菌活性和高生物安全性
论文链接://doi.org/10.1002/anie.5517893